Kalkulatori ya Tiger Algebra
Kupata uzito wa molekyuli
Uzito wa Molekyuli
Uzito wa molekyuli (pia unaitwa uzito wa atomic wa molekyuli, uzito wa formula, na uzito wa formula) inahusu uzito wa atomic uliochanganyika (pia unaitwa uzito wa atomic kawaida) wa atomi zinazounda molekyuli. Inaweza kupatikana kwa kuzidisha idadi ya atomi za kila elementi na uzito wao wa atomic na kuongeza matokeo pamoja.Kwa mfano, ina atomi mbili za Hydrojeni, kila mmoja na uzito wa atomic wa 1.008u, na atomi moja ya Oksijeni na uzito wa atomic wa 15.999u. Kutafuta uzito wa molekyuli ya , tunazidisha uzito wa atomic ya Hydrojeni kwa 2, kwa sababu kuna atomi mbili za Hydrojeni katika na tunahitaji kupata uzito wao uliochanganyika, na kuongeza kwa uzito wa atomic ya Oksijeni, kwa sababu kuna atomi moja tu ya Oksijeni katika , kupata 18.015u.
Uzito wa molekyuli unapimwa katika vitengo vya uzito wa atomic ulioratibiwa, ambavyo vinamezwa kama u. Bado sio kawaida kuona hivi vimeandikwa kama amu badala yake, kwani hii ilikuwa kifupisho cha zamani cha vitengo vya uzito wa atomic vilivyokubaliwa. Uzito wa molekyuli pia unaweza kupimwa kwa Daltoni, ambazo mara nyingi hupunguzwa kama Da.
Dhahania muhimu:
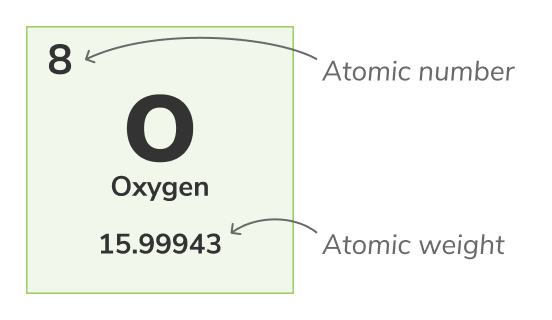
Idadi ya Atomic
Idadi ya Atomic - (pia inawaitwa idadi ya protoni) idadi ya protoni zilizopatikana katika kiini cha kila atomi ya elementi ya kikemia. Inatambua kipekee elementi ya kenkemikali, kwa mfano, atomi zote za Oksijeni zina protoni 8. Idadi ya Atomic kawaida inaonyeshwa juu ya vipengele katika jedwali la periodic.Idadi ya Misa
Idadi ya Misa - (pia inaitwa idadi ya atomic ya misa au idadi ya nucleon) inahusu idadi ya jumla ya protoni na nyutroni (pamoja inajulikana kama nucleons) katika kiini cha atomic. Elementi moja inaweza kuwa na aina tofauti za isotopu. Kwa mfano, Oksijeni inaweza kuwa na idadi ya misa ya au . Ina isotopu zake zote za protoni lakini idadi tofauti ya nyutroni, au mtawaliwa.Uzito wa Atomic
Uzito wa Atomic or - ni uzito wa atomi. thamani ya kimsingi ya uzito wa atomic ya atomi karibu sawa na thamani ya nambari yake ya uzito. Kwa mfano, uzito wa Oksijeni- ni 15.99491461956 u.Uzito wa Atomic
Uzito wa Atomic - (pia inaitwa uzito wa atomic kawaida) ni uzito wa kawaida wa isotopu zote za atomi. Kwa sababu isotopu zinatofautiana kwa uzito, uzito wa atomic kawaida unahesabiwa kwa kuchukua wastani wa uzito wa isotopu zote za atomi. Kwa mfano, Oksijen (O-16) atomi ni 99.762% ya atomi zote za Oksijeni, Oksijeni (O-17) atomi ni 0.038% ya atomi zote za Oksijeni na Oksijen (O-18) atomi ni 0.2% ya atomi zote za Oksijeni. Uzito wa atomic wa Oksijeni ni wastani wa isotopu zake 3 na inalingana na 15.99943 uUzito wa atomic unawakilishwa na idadi ya chini katika jedwali la periodic.