Kalkulator Tygrysiej Algebry
Znajdowanie masy cząsteczkowej
Masa cząsteczkowa
Masa cząsteczkowa (znana również jako masa molekularna, masa atomowa cząsteczki, masa formuły i masa formy) odnosi się do łącznej masy atomów tworzących cząsteczkę. Można ją wyznaczyć mnożąc liczbę atomów każdego pierwiastka przez ich masy atomowe i dodając razem uzyskane wyniki.Na przykład, zawiera dwa atomy wodoru, każdy o masie atomowej 1.008u, oraz jeden atom tlenu o masie atomowej 15.999u. Aby znaleźć masę cząsteczkową , mnożymy masy atomowe wodoru przez 2, ponieważ w są dwa atomy wodoru i musimy znaleźć ich łączną masę, a następnie dodajemy do tego masę atomową tlenu, ponieważ w jest tylko jeden atom tlenu, co daje 18.015u.
Masę cząsteczkową mierzy się w atomowych jednostkach masy, które są oznaczane jako u. Nie jest rzadkością, że zamiast tego stosuje się skrót amu, który był wcześniejszym skrótem od jednostek masy atomowej. Masę cząsteczkową można również mierzyć w daltonach, które często są oznaczane jako Da.
Powiązane terminy:
Liczba atomowa
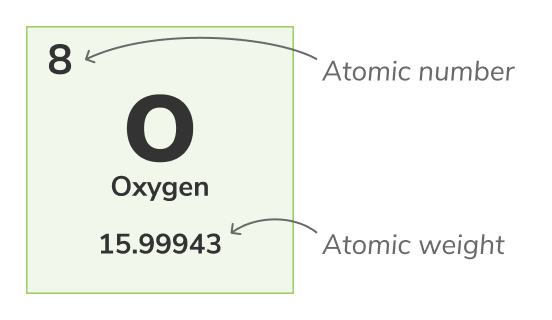
Liczba atomowa - (znana również jako liczba protonów) to liczba protonów znajdujących się w jądrze każdego atomu danego pierwiastka. Jednoznacznie identyfikuje ona pierwiastek chemiczny, na przykład wszystkie atomy tlenu mają 8 protonów. Liczba atomowa jest zazwyczaj pokazywana powyżej pierwiastków w tabeli okresowej.Liczba masowa
Liczba masowa - (zwana również liczbą mas atomowych lub liczbą nukleonów) odnosi się do łącznej liczby protonów i neutronów (znanych razem jako nukleony) w jądrze atomu. Jeden pierwiastek może mieć różne izotopy. Na przykład tlen może mieć liczbę masową or. Wszystkie jego izotopy mają protonów, ale różną liczbę neutronów, or odpowiednio.Masa atomowa
Masa atomowa or - to masa atomu. Wartość liczbową masy atomowej atomu jest niemal taka sama jak jego wartość liczby masowej. Na przykład, masa tlenu- wynosi 15.99491461956 u.Masa atomowa
Masa atomowa - (znana również jako standardowa masa atomowa) to średnia masa wszystkich naturalnych izotopów atomu. Ponieważ izotopy różnią się masą, standardową masę atomową oblicza się, biorąc średnią z mas wszystkich izotopów danego atomu. Na przykład, atomy tlenu (O-16) stanowią 99.762% wszystkich atomów tlenu, atomy tlenu (O-17) stanowią 0.038% wszystkich atomów tlenu, a atomy tlenu (O-18) stanowią 0.2% wszystkich atomów tlenu. Masa atomowa tlenu to średnia z jego 3 izotopów i wynosi 15.99943 uMasa atomowa jest reprezentowana przez dolny numer w tabeli okresowej.