ਟਾਈਗਰ ਐਲਜਬਰਾ ਕੈਲਕ੍ਯੁਲੇਟਰ
ਮੋਲੇਕਿਊਲਰ ਦਾ ਭਾਰ ਲੱਭਣਾ
ਮੋਲੇਕਿਊਲਰ ਭਾਰ
ਮੋਲੇਕਿਊਲਰ ਸ਼ਕਤੀ (ਜੋ ਇੱਕ ਮੋਲੇਕਿਊਲ ਦੀ ਪਰਮਾਣੂ ਸ਼ਕਤੀ, ਅਰਥ, ਮੱਗ ਅਤੇ ਚੱਕ ਦਾ ਰੋਗ ਵੀ ਕਹਿੰਦੇ ਹਨ) ਇੱਕ ਮੋਲੇਕਿਊਲ ਦਾ ਬਣਾਉਣ ਵਾਲੇ ਪਰਮਾਣੂ ਦੀ ਮਿਲਾਵਟ ਪਰਮਾਣੂ ਸ਼ਕਤੀ (ਜੋ ਆਮ ਪਰਮਾਣੂ ਵਜ਼ਨ ਵੀ ਕਹਿੰਦੇ ਹਨ) ਦਾ ਹੁੰਦਾ ਹੈ। ਇਸਨੂੰ ਹਰ ਤੱਤ ਦੇ ਪਰਮਾਣੂ ਦੀ ਗਿਣਤੀ ਨੂੰ ਉਹਨਾੰ ਦੀ ਪਰਮਾਣੂ ਸ਼ਕਤੀ ਨਾਲ ਗੁਣਨ ਕਰਨ ਤੇ ਨਤੀਜੇ ਨੂੰ ਜੋੜ੍ਹ ਕੇ ਪਾਇਆ ਜਾ ਸਕਦਾ ਹੈ।ਉਦਾਹਰਣ ਦੇ ਤੌਰ 'ਤੇ, ਵਿਚ ਦੋ ਹਾਈਡਰੋਜਨ ਪਰਮਾਣੂ ਹੁੰਦੇ ਹਨ, ਜਿਨ੍ਹਾਂ ਦਾ ਪਰਮਾਣੂ ਵਜ਼ਨ 1.008u ਹੁੰਦਾ ਹੈ, ਅਤੇ ਇੱਕ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਹੁੰਦਾ ਹੈ ਜਿਸਦਾ ਪਰਮਾਣੂ ਵਜ਼ਨ 15.999u ਹੁੰਦਾ ਹੈ। ਦਾ ਮੋਲੇਕਿਊਲਰ ਵਜ਼ਨ ਲੱਭਣ ਲਈ, ਅਸੀਂ ਹਾਈਡਰੋਜਨ ਦੀ ਪਰਮਾਣੂ ਸ਼ਕਤੀ ਨੂੰ 2 ਨਾਲ ਗੁਣਨ ਕਰਦੇ ਹਾਂ, ਕਿਉਂਕਿ ਵਿਚ ਦੋ ਹਾਈਡਰੋਜਨ ਪਰਮਾਣੂ ਹੁੰਦੇ ਹਨ ਅਤੇ ਸਾਡੇ ਕੋਲ ਉਨ੍ਹਾਂ ਦਾ ਜੋੜਾ ਭਾਰ ਲੱਭਣ ਦੀ ਲੋੜ ਹੈ, ਅਤੇ ਉਹਨੂੰ ਆਕਸੀਜਨ ਦੀ ਪਰਮਾਣੂ ਸ਼ਕਤੀ ਨਾਲ ਜੋੜਦੇ ਹਾਂ, ਕਿਉਂਕਿ ਇੱਕ ਹੀ ਵਿਚ ਇੱਕ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਹੁੰਦਾ ਹੈ, ਅਤੇ 18.015u ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਾਂ।
ਮੋਲੇਕਿਊਲਰ ਭਾਰ ਨੂੰ ਯੁਨਾਈਟਾਈਡ ਪਰਮਾਣੂ ਵਜ਼ਨ ਯੂਨਿਟਾਂ ਵਿਚ ਮਾਪਿਆ ਜਾਂਦਾ ਹੈ, ਜੋ ਕਿ u ਜਾਂ amu ਰੂਪ ਵਿਚ ਕੁਝ ਲਿਖੇ ਹੋਣ ਸ਼ਾਇਦ ਹੀ ਹੁੰਦੇ ਹਨ, ਕਿਉਂਕਿ ਇਹ ਯੁਨਾਈਟਾਈਡ ਪਰਮਾਣੂ ਵਜ਼ਨ ਯੂਨਿਟਾਂ ਦਾ ਪੂਰਾਣਾ ਸੰਕੇਤਨ ਸੀ। ਮੋਲੇਕਿਊਲਰ ਭਾਰ ਨੂੰ ਡਲਟਨਾਂ ਵਿਚ ਵੀ ਮਾਪਿਆ ਜਾ ਸਕਦਾ ਹੈ, ਜੋ ਕਿ ਡਾ ਰੂਪ ਵਿਚ ਅਕਸਰ ਲਿਖੇ ਜਾਂਦੇ ਹਨ।
ਸਬੰਧਤ ਸ਼ਬਦ:
ਪਰਮਾਣੂ ਨੰਬਰ
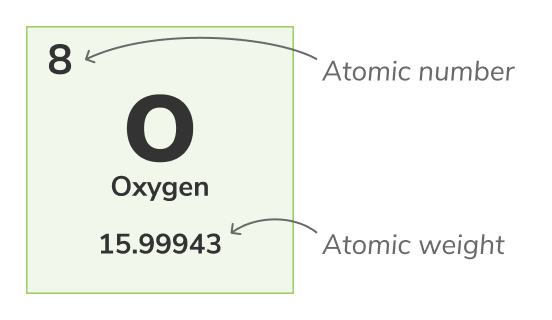
ਪਰਮਾਣੂ ਨੰਬਰ - (ਜੋ ਕਿ ਪ੍ਰੋਟੌਨ ਨੰਬਰ-ਵੀ ਕਹਿੰਦੇ ਹਨ) ਇੱਕ ਰਸਾਇਣਕ ਅੰਗ ਦੇ ਹਰ ਪਰਮਾਣੂ ਦੇ ਨੈਕਲੀਅਸ ਵਿਚ ਪਾਏ ਜਾਂਦੇ ਪ੍ਰੋਟਾਨਾਂ ਦੀ ਗਿਣਤੀ ਹੁੰਦੀ ਹੈ। ਇਹ ਇੱਕ ਰਸਾਇਣਕ ਤੱਤ ਦੀ ਨਿਜੀ ਪਹਿਚਾਣ ਬਣਦੀ ਹੈ, ਉਦਾਹਰਣ ਦੇ ਤੌਰ 'ਤੇ, ਸਾਰੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂ 8 ਪ੍ਰੋਟਾਨਾਂ ਰੱਖਦੇ ਹਨ। ਪਰਮਾਣੂ ਨੰਬਰ ਆਮ ਤੌਰ 'ਤੇ ਤੱਤਾਂ ਵਿਚ ਡਿਊਰਾਈਡ ਦੀਆਂ ਤਲੀਕਾਂ ਉੱਪਰ ਦਿਖਾਇਆ ਜਾਂਦਾ ਹੈ।ਭਾਰ ਨੰਬਰ
ਭਾਰ ਨੰਬਰ - (ਜੋ ਕਿ ਪਰਮਾਣੂ ਵਜ਼ਨ ਨੰਬਰ ਜਾਂ ਨਿਊਕਲੋਂ ਨੰਬਰ-ਵੀ ਕਹਿੰਦੇ ਹਨ) ਇੱਕ ਪਰਮਾਣੂ ਦੇ ਨੈਕਲੀਅਸ ਵਿਚ ਪ੍ਰੋਟਾਨ ਅਤੇ ਨਿਊਟ੍ਰਾਨ (ਜੋ ਨਿਊਕਲੋਨ ਵੀ ਕਹਿੰਦੇ ਹਨ) ਦੀ ਕੁੱਲ ਗਿਣਤੀ ਨੂੰ ਸ਼ੋਧ ਕਰਦਾ ਹੈ। ਇੱਕ ਤੱਤ ਵੱਖ ਵੱਖ ਪ੍ਰਕਾਰ ਦੇ ਆਇਸੋਟੋਪ ਜ਼ਾਹਿਰ ਕਰ ਸਕਦੇ ਹਨ। ਉਦਾਹਰਣ ਦੇ ਤੌਰ 'ਤੇ, ਆਕਸੀਜਨ ਦਾ ਭਾਰ ਨੰਬਰ ਜਾਂ ਹੋ ਸਕਦਾ ਹੈ। ਇਸਦੇ ਸਾਰੇ ਆਇਸੋਟੋਪਾਂ ਵਿਚ ਪ੍ਰੋਟਾਨ ਪਰ different ਨੰਬਰ ਦੇ ਨਿਊਟ੍ਰਾਨ, ਜਾਂ ਹੁੰਦੇ ਹਨ respectively.ਪਰਮਾਣੂ ਭਾਰ
ਪਰਮਾਣੂ ਭਾਰ ਜਾਂ - ਇੱਕ ਪਰਮਾਣੂ ਦਾ ਭਾਰ ਹੁੰਦਾ ਹੈ। ਪਰਮਾਣੂ ਦੇ ਭਾਰ ਦਾ ਨੈਮਰਿਕ ਮੁੱਲ ਉਸਦੇ ਭਾਰ ਨੰਬਰ ਦੀ ਮੁੱਲ ਨਾਲ ਲਗਭਗ ਇੱਕੋ ਹੁੰਦਾ ਹੈ। ਉਦਾਹਰਣ ਦੇ ਤੌਰ 'ਤੇ, ਆਕਸੀਜਨ- ਦਾ ਭਾਰ 15.99491461956 u ਹੁੰਦਾ ਹੈ।ਪਰਮਾਣੂ ਵਜ਼ਨ
ਪਰਮਾਣੂ ਵਜ਼ਨ - (ਜੋ ਕਿ ਆਮ ਪਰਮਾਣੂ ਵਜ਼ਨ-ਵੀ ਕਹਿੰਦੇ ਹਨ) ਇੱਕ ਪਰਮਾਣੂ ਦੇ ਸਾਰੇ ਪ੍ਰਾਕਤਿਕ ਆਇਸੋਟੋਪਾਂ ਦਾ ਔਸ਼ਤ ਵਜ਼ਨ ਹੁੰਦਾ ਹੈ। ਕਿਉਂਕਿ ਆਇਸੋਟੋਪਾਂ ਵਜ਼ਨ ਵਿਚ ਭਿੰਨ ਹੁੰਦੇ ਹਨ, ਆਮ ਪਰਮਾਣੂ ਭਾਰ ਇੱਕ ਪਰਮਾਣੂ ਦੇ ਸਾਰੇ ਆਇਸੋਟੋਪਾਂ ਦੇ ਭਾਰਾਂ ਦਾ ਔਸ਼ਤ ਲੈ ਕੇ ਅਦਾ ਅਨੁਸਾਰ ਗਣਾਂ ਕਰਦਾ ਹੈ। ਉਦਾਹਰਣ ਦੇ ਤੌਰ 'ਤੇ, ਆਕਸੀਜਨ (O-16) ਪਰਮਾਣੂ ਸਾਰੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਦੇ 99.762% ਹੁੰਦੇ ਹਨ, ਆਕਸੀਜਨ (O-17) ਪਰਮਾਣੂ ਸਾਰੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਦੇ 0.038% ਹੁੰਦੇ ਹਨ ਅਤੇ ਆਕਸੀਜਨ (O-18) ਪਰਮਾਣੂ ਸਾਰੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਦੇ 0.2% ਹੁੰਦੇ ਹਨ।The ਆਕਸੀਜਨ ਦਾ ਪਰਮਾਣੂ ਵਜ਼ਨ ਇਸਦੇ 3 ਆਇਸੋਟੋਪਾਂ ਦਾ ਔਸ਼ਤ ਹੈ ਅਤੇ 15.99943 u ਹੁੰਦਾ ਹੈ
The ਪਰਮਾਣੂ ਵਜ਼ਨ ਆਮ ਤੌਰ 'ਤੇ ਤਲੀਕਾ ਵਿਚ ਤੱਤ ਦੇ ਤਲੇ ਨੰਬਰ ਨਾਲ ਪ੍ਰਸਤੁਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ।