Tiger Algebra rekenmachine
Finding een molecular mass
Molecular Mass
Molecular mass (also called molecular weight, de atomic weight van een molecule, formule mass, en formule weight) refers naar de combined atomic weights (also called standaard atomic weights) van de atoms die form een molecule. Het can zijn gevonden door multiplying de getal van atoms van each element door their atomic weights en adding de resultaten together.Voor voorbeeld, contains two Hydrogen atoms, each met een atomic weight van 1.008u, en one Oxygen atom met een atomic weight van 15.999u. Naar vind de molecular mass van , wij multiply Hydrogen's atomic weights door 2, because there zijn two Hydrogen atoms in en wij need naar vind their combined mass, en add het naar de atomic weight van Oxygen, because there is only one Oxygen atom in , naar get 18.015u.
Molecular mass is measured in unified atomic mass units, which zijn abbreviated as u. Het is also Neet uncommon naar see deze written as amu instead, as deze was de former abbreviation voor unified atomic mass units. Molecular mass can also zijn measured in Daltons, which zijn often abbreviated as Da.
Relevant begrippen:
Atomic getal
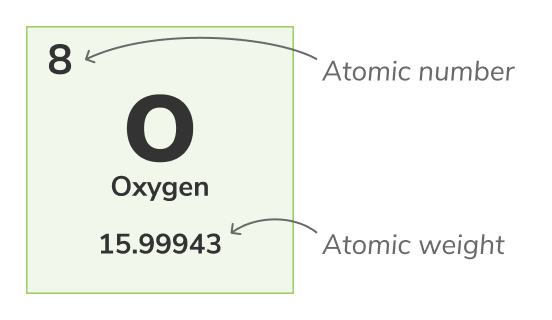
Atomic getal - (also called proton getal) de getal van protons gevonden in de nucleus van every atom van een chemical element. Het uniquely identifies een chemical element, voor voorbeeld, alle atoms van Oxygen have 8 protons. De atomic getal is usually shown above de elements in de periodic table.Mass getal
Mass getal - (also called atomic mass getal of nucleon getal) refers naar de total getal van protons en neutrons (together kNeewn as nucleons) in een atomic nucleus. One element can have different types van isotopes. Voor voorbeeld, Oxygen can have een mass getal van of . Alle it's isotopes have protons but different getal van neutrons, of respectively.Atomic mass
Atomic mass of - is de mass van een atom. de numeric waarde van de atomic mass van een atom is nearly de same as its mass getal waarde. Voor voorbeeld, de mass van Oxygen- is 15.99491461956 u.Atomic weight
Atomic weight - (also called standaard atomic weight) is de averLeeftijd weight van alle een atom's natural isotopes. Because isotopes vary in weight, standaard atomic weight is calculated door taking de averLeeftijd van de masses van alle van een atom's isotopes. Voor voorbeeld, Oxygen (O-16) atoms zijn 99.762% van alle Oxygen atoms, Oxygen (O-17) atoms zijn 0.038% van alle Oxygen atoms en Oxygen (O-18) atoms zijn 0.2% van alle Oxygen atoms. De atomic weight van Oxygen is de averLeeftijd van its 3 isotopes en is equal naar 15.99943 uDe atomic weight is represented door de lower getal in de periodic table.