Tiger Algebra Kalkulator
Paghahanap ng molekular na masa
Molekular na Masa
Ang molekular na masa (kilala rin bilang molekular na bigat, atomikong bigat ng isang molekula, masa ng formula, at bigat ng formula) ay tumutukoy sa pinagsamang atomikong mga bigat (kilala rin bilang standard na atomikong mga bigat) ng mga atomo na bumubuo sa isang molekula. Maaring matagpuan ito sa pamamagitan ng pagmu-multiply ng bilang ng mga atomo ng bawat elemento sa kanilang atomikong mga bigat at pagdadagdag ng mga resulta.Halimbawa, ang ay naglalaman ng dalawang mga atomong Hydrogen, bawat isa ay may atomikong bigat na 1.008u, at isang atomong Oxygen na may atomikong bigat na 15.999u. Para malaman ang molekular na masa ng , pinapalaki natin ang atomikong mga bigat ng Hydrogen sa 2, dahil mayroon itong dalawang atomo ng Hydrogen at kailangang malaman natin ang kanilang pinagsamang masa, at idinadagdag natin ito sa atomikong bigat ng Oxygen, dahil mayroong tanging isang atomo ng Oxygen sa , para makakuha ng 18.015u.
Ang molekular na masa ay sukatin sa mga yunit ng pinag-isang atomikong masa, na binabawasan bilang u. Hindi rin bihira na makita ang mga ito na sinulat bilang amu sa halip, dahil ito ang dating abbreviation para sa mga yunit ng pinag-isang atomikong masa. Maaari ring sukatin ang molekular na masa sa mga Dalton, na madalas na maikli bilang Da.
Mga may kaugnayan na termino:
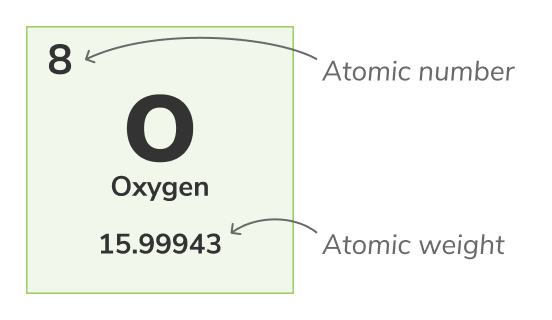
Atomic number
Atomic number - (tinatawag din na bilang ng proton) ang bilang ng mga proton na natagpuan sa nucleus ng bawat atomo ng isang kemikal na elemento. Tanging natutukoy nito ang isang kemikal na elemento, halimbawa, ang lahat ng mga atomo ng Oxygen ay may 8 na mga proton. Karaniwang ipinapakita ang atomic number sa itaas ng mga elemento sa talaan ng mga periodic.Bilang ng Masa
Bilang ng Masa - (tinatawag din na bilang ng atomikong masa o bilang ng nucleon) tumutukoy sa kabuuang bilang ng mga proton at neutron (kilala rin bilang mga nucleon) sa isang atomikong nucleus. Ang isang elemento ay maaaring magkaroon ng iba't ibang uri ng mga isotope. Halimbawa, ang Oxygen ay maaaring may bilang ng masa na o . Ang lahat ng isotops nito ay may na mga proton ngunit iba't ibang bilang ng mga neutron, o kahalintulad.Atomikong masa
Atomikong masa o - ito ang masa ng isang atomo. ang numeric na halaga ng atomikong masa ng isang atomo ay halos pareho sa halaga ng bilang ng masa nito. Halimbawa, ang masa ng Oxygen- ay 15.99491461956 u.Atomikong bigat
Atomikong bigat - (kilala din bilang standard na atomikong bigat) ito ang average na bigat ng lahat ng mga natural na isotopo ng isang atomo. Dahil nagkakalain-lain ang timbang ng mga isotopo, kalkulahin ang karaniwang atomikong bigat sa pamamagitan ng pagkuha ng average ng mga timbang ng lahat ng mga isotopo ng isang atomo. Halimbawa, Oxygen (O-16) mga atomo ay 99.762% ng lahat ng mga atomo ng Oxygen, Oxygen (O-17) mga atomo ay 0.038% ng lahat ng mga atomo ng Oxygen at ang Oxygen (O-18) mga atomo ay 0.2% ng lahat ng mga atomo ng Oxygen. Ang atomic weight ng Oxygen ay average ng 3 mga isotopo nito at ito'y pantay sa 15.99943 uAng atomikong bigat ay kinakatawan ng isa sa mga mababang bilang sa talaan ng mga periodic.