برنامج Tiger Algebra Calculator
البحث عن كتلة جزيئية
كتلة الجزيئات
تشير كتلة الجزيئات (والتي تُسمى أيضاً بالوزن الجزيئي، الوزن الذري للجزيء، وزن الصيغة، ووزن الصيغة) إلى وزن الذرات المجتمعة (والتي تُسمى أيضاً بالأوزان الذرية القياسية) اللتي تشكل الجزيء. يمكن العثور عليه بضرب عدد ذرات كل عنصر بوزنه الذري وجمع النتائج معًا.على سبيل المثال، يحتوي على ذرتي هيدروجين، كل منها بوزن ذري يبلغ 1.008u، وذرة أكسجين واحدة بوزن ذري يبلغ 15.999u. للعثور على كتلة الجزيئية، نضاعف أوزان الهيدروجين الذرية بمقدار 2، لأن هناك ذرتي هيدروجين في ونحتاج إلى العثور على كتلتها المجتمعة، ونضيفها إلى الوزن الذري للأكسجين، لأن هناك ذرة أكسجين واحدة فقط في ، للحصول على 18.015u.
تُقاس كتلة الجزيئات بوحدات الكتلة الذرية الموحدة، والتي يتم اختصارها باسم u. ليس من غير المألوف أيضًا رؤية هؤلاء مكتوبين كـ amu بدلاً من ذلك، حيث كانت هذه هي الاختصار السابق لوحدات الكتلة الذرية الموحدة. يمكن أيضًا قياس كتلة الجزيئات بالدالتون، التي غالباً ما يتم اختصارها كـ Da.
المصطلحات ذات الصلة:
العدد الذري
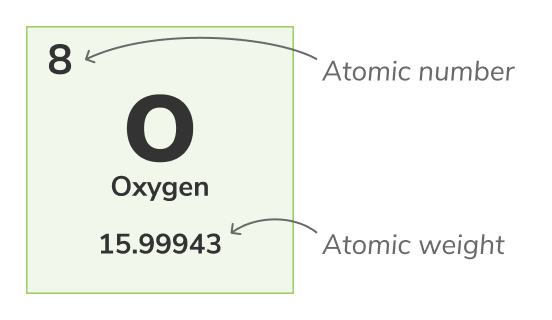
العدد الذري - (يُعرف أيضاً بالعدد البروتوني) العدد الذي يمثل البروتونات الموجودة في نواة كل ذرة من ذرات العنصر الكيميائي. يتم التعرف على العنصر الكيميائي بشكل فريد، على سبيل المثال، يحتوي كل ذرات الأكسجين على 8 بروتونات. يتم عادة عرض العدد الذري فوق العناصر في الجدول الدوري.رقم الكتلة
رقم الكتلة - (يُعرف أيضاً برقم الكتلة الذرية أو رقم النويتدون) يشير إلى العدد الإجمالي للبروتونات والنيوترونات (المعروفة معا بالنوكليونات) في نواة الذرة. يمكن أن يكون للعنصر أنواع مختلفة من النظائر. على سبيل المثال، يمكن أن يكون رقم الكتلة للأكسجين أو . جميع نظائر الأكسجين لديها بروتونات ولكن عدد مختلف من النيترونات، أو .الكتلة الذرية
الكتلة الذرية or - هي كتلة الذرة. القيمة العددية للكتلة الذرية للذرة تقريباً نفسها كقيمة رقم الكتلة. على سبيل المثال، الكتلة الذرية لأكسجين - هي 15.99491461956 u.الوزن الذري
الوزن الذري - (يُعرف أيضاً بالوزن الذري القياسي) هو وزن متوسط جميع نظائر الذرة الطبيعية. نظراً لأن النظائر تختلف في الوزن، يتم حساب الوزن الذري القياسي عن طريق أخذ المتوسط لكتل جميع نظائر الذرة. على سبيل المثال، ذرات الأكسجين (O-16) تشكل 99.762% من جميع ذرات الأكسجين، وذرات الأكسجين (O-17) تشكل 0.038% من جميع ذرات الأكسجين وذرات الأكسجين18 (O-18) هي 0.2% من جميع ذرات الأكسجين. الوزن الذري للأكسجين هو المتوسط لالثلاث نظائر ويساوي 15.99943 uيتم تمثيل الوزن الذري من قبل الرقم الأدنى في الجدول الدوري.